Какого ребенка считать часто болеющим, и чем ему грозит вирус Эпштейна-Барр?
Буквально каждая вторая современная мама, словно мантру, заучила формулировку «часто болеющий ребенок», но что это значит, известно не всем. Почему он часто болеет, чем это грозит, и что за странные анализы назначают врачи? Такие вопросы нередко рождаются в головах испуганных родителей.
Пролить свет истины на эту тему пресс-службе Интернет-Портала NEDUGAMNET.RU помогла Ксения Борисовна Степанова, к.м.н., врач-инфекционист, заведующий клиникой ФБУН «Тюменский научно-исследовательский институт краевой инфекционной патологии».
Для начала Ксения Борисовна рассказала о том, в каких случаях можно с уверенностью сказать, что ребенок болеет слишком часто.
«Если ребенок возрастом до 3 лет болеет 5-6 раз – это норма, для ребенка 5-14 в норме болеть не более 4 раз в год. Однако это справедливо лишь для случаев, когда дети болеют без осложнений.
Когда болеют пять раз легкими простудами, это одна ситуация, которая не так страшна, чем когда ребенок за год все 4 раза подхватывал тяжелые инфекционные заболевания, а итогом стали осложнения: гайморит, аденоиды, менингит и т.д. В последнем случае вероятность иммунодефицита очень высока», – пояснила врач-инфекционист.
Также она уточнила, что причина частых заболеваний у ребенка кроется в неадекватном иммунном ответе на внедрение инфекционного агента. Причиной такого неадекватного ответа иммунной системы могут быть как паразиты, так и хронические вирусные инфекции, в том числе вирус Эпштейна-Барр.
Анализ на выявление этого вируса в организме могут назначить часто болеющему ребенку, что нередко пугает родителей.
«Эпштейна-Барр (ВЭБ) – вирус герпеса, который впервые был обнаружен у больного с онкопатологией (лимфома Беркитта) 35 лет назад. Может стать причиной как острых инфекционных заболеваний (например, инфекционного мононуклеоза, так и хронического течения данной инфекции. Также ВЭБ может приводить к ряду онкологических и аутоиммунных заболеваний.
ВЭБ может пожизненно находится в организме человека, поражая b-лимфоциты иммунной системы, которые в основном находятся в миндалинах. По этой причине во внешнюю среду вирус выделяется чаще всего со слюной.
Врожденная Эпштейна-Барр-вирусная инфекция, пожалуй, дает самые серьезные осложнения – ребенок изначально рождается с различными патологиями: с гепатитом С, энцефалитом, различными повреждениями кожного покрова. Хотя такие случаи редки в медицинской практике.
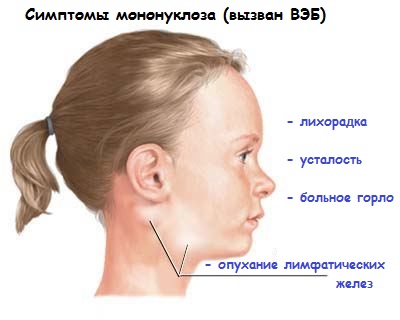
Самое типичное проявление вируса Эпштейна-Барр – это инфекционный мононуклеоз, острое инфекционное заболевание, которое протекает с выраженной интоксикацией, с поражением лимфатических узлов, возможным увеличением печени, селезенки и даже развитием в тяжелых случаях острого гепатита.
Хроническая Эпштейна-Барр-вирусная инфекция характеризуется длительным рецидивирующим течением и наличием признаков вирусной активности (боли в мышцах, суставах, высыпания, затрудненное дыхание, боли в горле, головные боли, часто наблюдается субфебрильная температура).
У лиц с выраженной иммунной недостаточностью могут возникнуть генерализованные формы ВЭБ-инфекции с развитием менингита и энцефалита, а также миокардита. Для ВЭБ-инфекции характерно развитие анемии и панцитопении (снижается уровень лейкоцитов и тромбоцитов).
Диагностика ВЭБ-инфекции достаточно сложна и трудоемка, диагноз может поставить только врач-инфекционист после проведения анализов – исследования крови или мочи (ИФА и ПЦР)», – пояснила Ксения Борисовна.
Она отметила, что есть несколько категорий пациентов среди детского населения, которым рекомендовано сдавать анализ на выявление вируса:
· пациенты с частыми респираторными заболеваниями, с любыми иммунодефицитными состояниями;
· дети с долговременной температурой субфебрильного характера либо жалобами на беспричинное повышение температуры тела;
· дети с увеличенными лимфоузлами;
· пациенты с отклонениями в общем анализе крови;
· пациенты, у которых обнаруживаются неустановленные заболевания печени;
· все пациенты с диагнозом ВИЧ;
· все, кто перенес пересадку органов или переливания крови и ее компонентов.
«У этого вируса нет сезонности, он распространен повсеместно, передается воздушно-капельным путем. Также вирус Эпштейна-Барр называют «болезнью поцелуев» или «студенческой болезнью», потому как этим заболеванием можно заразиться в том числе контактно-бытовым путем, через слюну.
Лечение требуется как острой инфекции, так и хронической, но в определенной стадии заболевания. Подход к лечению строго индивидуальный с подбором противовирусной терапии. Учитывается возраст пациента, длительность течения заболевания и клиническая картина. Иногда при хронической ВЭБ-инфекции пациент вынужден наблюдаться у специалистов длительное время и даже пожизненно», – рассказала врач-инфекционист Ксения Борисовна Степанова.
Источник
ВИРУС ЭПШТЕЙН-БАРРА У ДЕТЕЙ. ЧТО ЭТО ТАКОЕ?
ВИРУС ЭПШТЕЙН-БАРРА У ДЕТЕЙ. ЧТО ЭТО ТАКОЕ.
Малыши часто болеют вирусными заболеваниями, и некоторые из них несут серьезную угрозу для здоровья детей. В настоящий момент педиатры всего мира обращают особое внимание на патологии, что вызывает вирус Эпштейн-Барра.
Инфекционный мононуклеоз – это болезнь вирусной этиологии. Инфекционный агент –герпесоподобный вирус Эпштейн-Барра, способный вызывать не только инфекционный мононуклеоз, но и провоцировать развитие носоглоточной карциномы, лимфомы Беркитта и, вероятно, ряд иных заболеваний. Статистика свидетельствует о том, что это заболевание наиболее часто встречается у детей. Мононуклеоз у детей – это очень распространенная инфекция: до достижения пятилетнего возраста каждый второй ребенок уже заражен патологией. Однако развивается заболевание примерно у 5%детей, а во взрослом возрасте встречается крайне редко в связи с особенностями иммунной системы.
При первичном заражении у ребенка симптомы этой инфекции могут остаться незамеченными. Последствия инфекции спустя несколько месяцев негативно влияют на все органы и системы организма. Что нужно знать родителям о признаках этой болезни?
Вирус Эпштейна-Барр (ВЭБ) –возбудитель ряда заболеваний человека, принадлежит группе вирусов герпеса (иное название – инфекционный агент герпеса 4 типа). Открыт в 1964 году в Великой Британии учеными Михаэлем Эпштейном и Ивонной Барр. Размножается в клетках иммунной системы ребенка (лимфоцитах) и вызывает их неконтролируемый рост
Вирус имеет в своем составе такие элементы, против которых в телах детей В-лимфоцитами вырабатываются антитела классов IgM и IgG (иммуноглобулин М, G):
· VCA –капсидный антиген;
· ENBA –ядерный антиген;
· EA – ранний антиген.
Когда в крови ребенка обнаружен IgM и IgG (иммуноглобулин М, G) против вышеуказанных антигенов (VCA,EA, ENBA), если проводится серологический анализ, то можно диагностировать острую или хроническую форму заболевания, вызванного вирусом Эпштейна-Барр.
Признаки и симптомы
Рассмотрим симптомы инфекционного мононуклеоза, который является проявлением первичного контакта ребенка с вирусом Эпштейна-Барр. Иногда мононуклеоз у детей вызывает цитомегаловирус (ЦМВ; дифференциальный серологический анализ всегда необходим).Заболевание начинается остро и длится от 3 до 4 недель.
При мононуклеозе (если его причина ВЭБ, а не цитомегаловирус) проявляется следующая симптоматика. Её обнаруживают при непосредственном осмотре ребенка:
1. Повышение температуры тела до 39-40 градусов с тяжелым интоксикационным синдромом –тошнота, рвота, слабость, головная боль, тахикардия;
2. Увеличение лимфатических узлов по всему телу (особенно на шее – передне- и заднешейные узлы);
3. Назофарингит и тонзиллит с бело-серыми или желтоватыми налетами (из-за поражения небных миндалин и аденоидов);
4. Утрудненное носовое дыхание при отсутствии выделений из носовых ходов, одутловатость лица,гнусавость голоса;
5. Увеличение печени и селезенки (гепатоспленомегалия у детей), боли в брюшной полости,иктеричность склер и кожи;
6. Экзантема(высыпания вирусного происхождения) в виде пятен, папул, везикул с повсеместной локализацией.
При микроскопическом исследовании в период острой инфекции среди обычных кровяных клеток находят большие атипичные лимфоциты, что поражены вирусом, –мононуклеары (такую картину крови иногда дает цитомегаловирус, ЦМВ). Они сохраняются в кровяном русле на протяжении месяца с момента заражения.
Для серологической диагностики мононуклеоза используют иммуноферментный анализ(ИФА) или полимеразноцепную реакцию (ПЦР), с помощью какой выявляют вирус Эпштейна-Барра.
Какие антитела (АТ) типов IgG и IgM (иммуноглобулин М, G) являются диагностическими, когда проводят ИФ-анализ?
Анти-VCA антитела класса IgM (иммуноглобулин М к капсидному антигену)
Вырабатываются при острой ВЭБ-инфекции, циркулируют в крови 2-3 месяца. Повторно синтезируются в случае реактивации вируса.
Высокая концентрация анти-VCA IgM, что длительно сохраняется, – свидетельство хронической формы ВЭБ.
Анти-EA антитела класса IgG (иммуноглобулин G к раннему антигену)
Появляются в крови на 3-4 неделе от начала острой ВЭБ-инфекции, сохраняются в течение 2-6 месяцев. Вновь анти-EA IgG появляются при реактивации возбудителя.
Анти-EBNA антитела класса IgG (иммуноглобулин G к ядерному антигену)
Начинают циркулировать в кровяном русле через 1-6 месяцев после первичного ВЭБ-заболевания. Постепенно их концентрация уменьшается. Анти-EBNA IgG может быть обнаружен до конца жизни человека (их всегда выявляет ИФ-анализ).
Если был проведен ИФ-анализ, положительный результат, выявивший:
· антителатипа IgG (иммуноглобулин G) против ядерного и ранних антигенов;
· антителатипа IgM (иммуноглобулин М) к капсидному (VCA) антигену вируса
Профилактика
1. Для того, чтобы избежать заражения вирусом Эпштейна-Барр с ранних лет приучайте ребенка к личной гигиене.
2. В осеннее-зимнее время избегайте больших скоплений людей, так как при чихании и кашле тоже существует вероятность передачи возбудителя Эпштейн-Барр.
3. Ведите здоровый образ жизни, так как вирус Эпштейн-Барра после попадания в организм может длительное время находится в нем в латентной форме (симптомы появляются при ослаблении иммунитета, физическом истощении, если прервано лечение иной болезни).

Мы заботимся о вашем здоровье и здоровье ваших детей!
Источник
Вирус Эпштейн — Барр и аутоиммунные заболевания
Опубликовано вс, 27/12/2020 — 18:18
Заражения вирусом Эпштейн — Барр
Вирус Эпштейн — Барр — это широко распространенный вирус герпеса человека, который обладает уникальной способностью инфицировать, активировать и латентно сохраняться в В-лимфоцитах на протяжении всей жизни инфицированного человека. Во время первичной инфекции EBV , передаваемый через слюну, поражает нативные В-клетки в миндалинах путем связывания поверхностного гликопротеина вируса gp350 с рецептором комплемента 2 (также известным как CD21), который экспрессируется зрелыми В-клетками и фолликулярными дендритными клетками .
В развивающихся странах большинство детей инфицируются в течение первых трех лет жизни, и серопозитивность по EBV достигает 100% в течение первого десятилетия. Эти ранние первичные инфекции почти всегда протекают бессимптомно. Напротив, в развитых странах до половины детей все еще остаются серонегативными по EBV в конце своего первого десятилетия жизни и впоследствии заражаются при интимном оральном контакте в подростковом или юношеском возрасте. До 50% этих отсроченных первичных инфекций носят симптоматический характер и проявляются как острый инфекционный мононуклеоз. Когда первичная инфекция EBV возникает в раннем детстве, как это обычно бывает в развивающихся странах, она протекает бессимптомно, но когда она откладывается до подросткового возраста или позже, как в развитом мире, она обычно проявляется. как инфекционный мононуклеоз, при котором количество латентно инфицированных В-клеток памяти может возрасти до половины, а возможно, даже выше, от компартмента периферических В-клеток памяти. Неясно, почему следует инфицировать более высокую долю В-клеток, если первичная инфекция откладывается от детства до подросткового возраста или позже. Возможные объяснения включают более высокую дозу вирусного инокулята, полученного при интимном оральном контакте, и пониженную способность вызывать быстрый эффективный CD8 + Т-клеточный ответ у подростков / взрослых по сравнению с маленькими детьми.
Диагностика инфекции вирусом Эпштейн — Барр
Золотым стандартом для обнаружения EBV-инфицированных B-клеток в гистологическом материале является гибридизация in situ для кодируемой EBV малой РНК (EBER-ISH) , что позволяет определять частоту В-клеток, инфицированных вирусом гепатита В, в инфильтратах В-клеток. Однако, если вирусная нагрузка ткани определяется как общее количество копий генома EBV, определенное с помощью полимеразной цепной реакции (ПЦР), то невозможно определить, является ли значительное увеличение вирусной нагрузки результатом большого увеличения частоты латентно инфицированные В-клетки, которые экспрессируют от двух до пяти копий вирусного генома на клетку, или очень небольшого увеличения доли инфицированных клеток, реплицирующих вирус, которые содержат тысячи геномов на клетку. На вероятность обнаружения EBV в органе-мишени также влияет размер образца ткани, при этом вероятность обнаружения при биопсии ниже, чем при исследовании всего органа
Исследования с использованием EBER-ISH выявили повышенную частоту EBV-инфицированных В-клеток в слюнных железах при синдроме Шегрена , толстой кишке при язвенном колите и болезни Крона , головном мозге при рассеянном склерозе , тимусе при миастении и щитовидной железе при болезни Грейвса. Исследования с использованием только ПЦР показали повышенные уровни ДНК EBV в печени при первичном билиарном циррозе , почках при IgA-нефропатии и мембранозной нефропатии и легких при идиопатическом фиброзе легких. В то время как концепция органа-мишени ясна для органоспецифического аутоиммунитета, это менее ясно для системного аутоиммунитета. При системной красной волчанке например, повреждение ткани может быть опосредовано либо аутоантителами, продуцируемыми в лимфоидных органах, удаленных от ткани-мишени, либо прямой лимфоцитарной инфильтрацией нелимфоидных органов, таких как почки.
Абсолютный размер популяции CD8 + Т-клеток у здоровых людей уменьшается в три раза в возрасте от 2 до 16 лет Здесь предполагается, что генетически детерминированный дефицит Т-лимфоцитов CD8 + не ведет к нарушению контроля над EBV , когда первичная инфекция происходит в раннем детстве, если дефицит не является серьезным, но когда первичная инфекция происходит в подростковом или взрослом возрасте после нормального возраста — связанное с этим резкое снижение количества CD8 + Т-клеток и тот же генетический дефицит CD8 + Т-клеток с большей вероятностью ухудшит контроль над инфекцией EBV.
Вирус Эпштейн — Барр и В — клетки
EBV выводит инфицированную В-клетку из состояния покоя и превращает ее в активированный В-бласт, а затем использует нормальные пути дифференцировки В-клеток, так что В-бласт дифференцируется в зародышевом центре и становится латентно инфицированной В-клеткой памяти покоя, которая выходит из зародышевого центра и циркулирует в крови. Латентно инфицированные В-клетки памяти, возвращающиеся в миндалины, могут окончательно дифференцироваться в плазматические клетки, которые инициируют литический (репликативный) цикл с образованием инфекционного вируса. Полученные в результате свободные вирионы инфицируют эпителиальные клетки миндалин, где вирус реплицируется с высокой скоростью и постоянно выделяется в слюну для передачи новым хозяевам. Новообразованный вирус также может инфицировать дополнительные нативные В-клетки у того же хозяина.
Латентно инфицированные В-клетки памяти обнаруживают молекулярные признаки классических антиген-отобранных В-клеток памяти, а именно соматическую гипермутацию и рекомбинацию их иммуноглобулиновых (Ig) генов с переключением классов. При нормальной дифференцировке B-клеток нативные B-клетки активируются антигеном через B-клеточный рецептор (BCR) и с помощью T-клеток через рецептор CD40, так что они пролиферируют и прогрессируют через реакцию зародышевого центра. Примечательно, что EBV экспрессирует два белка, латентный мембранный белок 2A (LMP2A) и LMP1, которые имитируют активированный антигеном BCR и активированный рецептор CD40 соответственно. В миндалинах LMP2A и LMP1, по-видимому, работают синергетически с передачей сигналов BCR и CD40, соответственно
Экспансия моноклональных или олигоклональных B-клеток происходит в щитовидной железе при тиреоидите Хашимото , слюнных железах при синдроме Шегрена , синовиальной оболочке при ревматоидном артрите , спинномозговой жидкости при рассеянном склерозе , печени при первичном билиарный цирроз, мышцы при дерматомиозите и полимиозите и кровь при системной красной волчанке. Эти клонально размноженные В-клетки демонстрируют молекулярные признаки реакции зародышевого центра, управляемой антигеном, а именно соматическую гипермутацию и высокое соотношение мутаций замещения к молчащим мутациям в определяющих комплементарность областях генов вариабельной (V) области Ig.
Вирус Эпштейн — Барр и Т — клетки
Инфекция EBV обычно находится под жестким контролем EBV-специфических иммунных ответов, особенно цитотоксических CD8 + T-клеток, которые устраняют пролиферирующие и литически инфицированные B-клетки. Контроль CD8 + Т — клеток из EBV-инфицированных В — клеток нарушается у пациентов с аутоиммунными заболеваниями. При рассеянном склерозе этот дефектный контроль EBV не связан с повышенной устойчивостью B-клеток к уничтожению цитотоксическими CD8 + T-клетками или с функциональным нарушением цитотоксической способности CD8 + T-клеток, а является результатом уменьшения количества EBV-специфичных CD8 + T-клеток. Это, в свою очередь, происходит из-за общего дефицита CD8 + T-клеток и из-за уменьшения доли EBV-специфических T-клеток в общей популяции CD8 + T-клеток. Было высказано предположение, что низкая доля EBV-специфических Т-клеток в популяции CD8 + Т-клеток при рассеянном склерозе связана с истощением Т-клеток, которое происходит в вирус-специфических CD8 + Т-клетках во время хронических вирусных инфекций высокой степени тяжести. Лишение солнечного света и витамина D также усугубит дефицит CD8 + Т-клеток и нарушение контроля EBV
Вирус Эпштейн — Барр и аутоиммунные заболевания
Вирус Эпштейна-Барра (EBV) подозревался в участии в патогенезе различных хронических аутоиммунных заболеваний с момента обнаружения повышенных уровней антител к этому вирусу при системной красной волчанке (СКВ) в 1971 году. Обычно эффект инфекции EBV объясняется иммунологической перекрестной реактивностью между EBV и аутоантигенами. Однако в 2003 г. гипотеза аутоиммунных заболеваний, связанных с инфицированием EBV, была предложена в качестве основы для этиопатогенеза хронических аутоиммунных заболеваний человек. Эта гипотеза предполагает, что у генетически предрасположенных индивидуумов аутореактивные В-клетки, инфицированные EBV , засевают орган-мишень, где они вырабатывают патогенные аутоантитела и обеспечивают костимулирующие сигналы выживания аутореактивным Т-клеткам, которые в противном случае умерли бы в органе-мишени в результате индуцированного активацией апоптоза. Вероятно, предрасположенность к развитию хронических аутоиммунных заболеваний после инфицирования EBV зависит от генетически детерминированного количественного дефицита цитотоксических CD8 + Т-клеток, которые обычно держат инфекцию EBV под жестким контролем.
С 1980 годом было признано , что доля и количество CD8 + Т — клеток в периферической крови уменьшаются , и что отношение CD4 / CD8 увеличивается у пациентов с аутоиммунными заболеваниями, в том числе при рассеянном склерозе (MS), ревматоидном артрите , системной красной волчанке , синдроме Шегрена , системном склерозе , дерматомиозите , первичном билиарном циррозе , первичном склерозирующем холангите , язвенном колите , болезни Крона, псориазе, витилиго , буллезном пемфигоиде , очаговой алопеции , идиопатической дилатационной кардиомиопатии , сахарном диабете 1 типа, болезни Грейвса , тиреоидите Хашимото , миастении, нефропатии IgA , мембранозной нефропатии (или мембранозном гломерулонефрите) и пернициозной анемии.
Таким образом, дефицит CD8 + T-клеток, по-видимому, является общей характеристикой хронических аутоиммунных заболеваний человека. Первоначально это было интерпретировано как уменьшение количества супрессорных CD8 + Т-клеток, приводящее к растормаживанию аутоиммунных ответов, но позже это было связано с секвестрацией CD8 + Т-клеток в органе-мишени, поскольку CD8 + Т-клетки избирательно обогащены по сравнению с CD4 + Т-клетками в целевом органе при некоторых аутоиммунных заболеваниях. Однако, если CD8 + Т-клетки накапливаются в органе-мишени из-за присутствия EBV, количество CD8 + T-клеток в крови должно увеличиваться, а не уменьшаться, потому что обычно ответ CD8 + T-клеток увеличивается с нагрузкой EBV. Альтернативное объяснение, состоит в том, что генетический дефицит CD8 + Т-клеток приводит к снижению ответа CD8 + Т-клеток на EBV, что позволяет В-клеткам, инфицированным EBV, накапливаться в органе-мишени.
Профилактика аутоиммунных заболеваний
Вакцинация здоровых ВИЧ-серонегативных молодых людей рекомбинантным gp350 эффективна для предотвращения развития инфекционного мононуклеоза, вызванного EBV-инфекцией, хотя и не предотвращает бессимптомную EBV-инфекцию, но вакцинированные субъекты показали сероконверсию к антителам против gp350, которые сохранялись> 18 месяцев и, вероятно, были ответственны за защитный эффект, поскольку антитело против gp350 нейтрализует инфекционность EBV Вакцинация gp350 может снизить частоту хронических аутоиммунных заболеваний за счет уменьшения количества В-клеток, инфицированных EBV , и тем самым уменьшения вероятности инфицирования аутореактивных В-клеток во время первичной инфекции.
Лечение аутоиммунных заболеваний
Потенциально существует три способа лечения хронических аутоиммунных заболеваний путем борьбы с инфекцией EBV: (1) истощение В-клеток моноклональными антителами; (2) повышение иммунитета к EBV; (3) противовирусные препараты. Истощение В-клеток ритуксимабом уничтожает не только В-клетки, инфицированные EBV , но и неинфицированные В-клетки, которые обычно обеспечивают защитный иммунитет против инфекционных агентов. Улучшение nтечения аутоиммунного заболевания с помощью терапии ритуксимабом согласуется с важной ролью EBV в развитии заболевания, но не является доказательством, поскольку положительный эффект может быть опосредован элиминацией аутореактивных B-клеток, не инфицированных EBV. Более убедительным доказательством важной роли EBV может быть искоренение аутоиммунных заболеваний путем повышения иммунитета к EBV или лечения противовирусными препаратами. Гуморальный иммунитет к EBV может быть усилен вакцинацией gp350 или введением гуманизированного или человеческого моноклонального антитела против gp350. CD8 + Т-клеточный иммунитет может быть усилен внутривенной инфузией аутологичных EBV-специфических цитотоксических CD8 + Т-клеток после размножения in vitro или введением таких агентов, как интерлейкин-7, который увеличивает популяцию функциональных вирус-специфических CD8 + Т-клеток при хронической вирусной инфекции.
Что касается противовирусных препаратов, лечение ацикловиром и родственными ему препаратами, которые ингибируют ДНК-полимеразу герпесвируса, вероятно, будет иметь лишь ограниченный положительный эффект при хронических аутоиммунных заболеваниях, потому что эти препараты действуют на EBV только тогда, когда он использует свою собственную ДНК-полимеразу для репликации своей ДНК. Это применимо только к литически инфицированным клеткам, но не к латентно инфицированным, которые реплицируют ДНК EBV за счет использования ядерного антигена 1 EBV (EBNA1) для взаимодействия с ДНК-полимеразой клетки-хозяина. Одна из стратегий преодоления этого — сначала введение ритуксимаба для уничтожения как можно большего количества В-клеток, инфицированных EBV , и последующая длительная противовирусная лекарственная терапия. Альтернативный подход — нацеливаться на LMP1 , LMP2A или EBNA1 для подавления EBV в латентно инфицированных клетках. Было также высказано предположение, что ингибиторы ретровирусной интегразы могут быть эффективными против EBV при аутоиммунных заболеваниях.
Генетические аспекты иммунорегуляторного индекса
Соотношение CD4 / CD8 Т-клеток у человека контролируется генетически , при этом по крайней мере некоторые ответственные гены расположены в комплексе HLA. Дефицит CD8 + Т-клеток и повышенное соотношение CD4 / CD8 при аутоиммунных заболеваниях также присутствуют у здоровых кровных родственников пациентов с этими заболеваниями, что указывает на то, что отклонения являются генетически детерминированными, а не вторичными по отношению к ним.
Гормональные аспекты иммунорегуляторного индекса
Интересно, что у женщин обычно более низкие пропорции и количество CD8 + Т-клеток, более высокие пропорции и количество CD4 + Т-клеток и более высокое соотношение CD4 / CD8, чем у мужчин. Эти гендерные различия, по-видимому, опосредованы гормонами, потому что дефицит эстрогенов существенно увеличивает долю и количество CD8 + Т-клеток и снижает соотношение CD4 / CD8, причем это соотношение напрямую коррелирует с уровнем эстрадиола в сыворотке. Более низкое количество CD8 + Т-клеток у женщин может способствовать более высокой частоте аутоиммунных заболеваний у женщин, чем у мужчин.
Возрастные аспекты иммунорегуляторного индекса
Поскольку количество CD8 + Т-лимфоцитов обычно снижается с возрастом, особенно в детстве , но также и в зрелом возрасте , первичный дефицит CD8 + Т-клеток будет усугубляться с возрастом каждого человека, как это происходит у пациентов. с рассеянным склерозом.
Экологические факторы , витамин D и иммунорегуляторный индекс
Воздействие естественного солнечного света или лечение в солярии увеличивает долю CD8 + Т-клеток и снижает соотношение CD4 / CD8 Т-клеток в периферической крови. Неясно, как именно солнечный свет увеличивает количество CD8 + T-клеток, но эффект, вероятно, опосредован, по крайней мере частично, витамином D, потому что (1) среди клеток иммунной системы активированные CD8 + T-клетки экспрессируют самые высокие концентрации рецептора витамина D. (2) витамин D увеличивает индуцированную митогеном пролиферацию CD8 + Т-клеток и снижает соотношение CD4 / CD8 в мононуклеарных клетках периферической крови крупного рогатого скота in vitrо. (3) прием витамина D увеличивает количество CD8 + Т-лимфоцитов. (4) дефицит витамина D связан со снижением доли CD8 + Т-клеток и повышенным соотношением CD4 / CD8. Здесь предполагается, что лишение солнечного света и витамина D усугубляет генетически обусловленный дефицит Т-лимфоцитов CD8 + и нарушает контроль инфекции EBV и тем самым способствует высокой распространенности аутоиммунных заболеваний, таких как рассеянный склероз , диабет 1 типа и ревматоидный артрит , в высоких широтах и что защитный эффект витамина D против аутоиммунных заболеваний , по крайней мере частично, опосредуется увеличением количества CD8 + Т-клеток, доступных для контроля EBV. Более высокая частота поздней первичной инфекции EBV на более высоких широтах также может вносить вклад в широтный градиент
Источник

